
Wichtigstes
Problem: Wie entstehen Fettsäuren?
Dreh- und Angelpunkt des Ganzen ist das Acetyl-CoA. Wir haben
es als ein Verbindungsglied zwischen Glykolyse und Citratzyklus
kennengelernt. In Chloroplasten scheint es noch einige weitere
Möglichkeiten zu seiner Synthese zu geben, über dessen
Mechanismus jedoch noch etliche Unklarheiten bestehen. Im Cytoplasma
kann es auch unter ATP-Verbrauch aus Citrat gebildet werden (Umkehr
des entsprechenden ersten Schrittes des Citratzyklus).
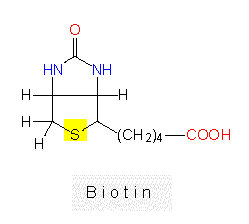
Zum Start der Fettsäuresynthese wird Acetyl-CoA unter Kohlendioxyd-Anlagerung in Malonyl-CoA überführt. Der dafür erforderliche Kofaktor ist proteingebundenes Biotin. Der für unsere Zwecke benötigte Kofaktor-Proteinkomplex ist in grünen Pflanzen in den Thylakoidmembranen der Chloroplasten und in Samen (oder ethiolierten, chlorophyllfreien Formen) in den Proplastiden lokalisiert. Um in der Fettsäuresynthese weiterzukommen, brauchen wir wieder beides: Acetyl-CoA und Malonyl-CoA.Beide Reste werden unter CoA-Abspaltung auf je ein Acyl-Trägerprotein (ACP) übertragen.
In so aktiviertem Zustand kondensieren sie miteinander, wobei Kohlendioxyd und einer der ACP-Reste abgespalten werden. Anschließend folgt eine Reduktion, dann eine Dehydrierung, und schließlich wieder eine Reduktion. In beiden Reduktionsschritten werden die Elektronen vom NADPH + H+ geliefert. Als Produkt entsteht Butyryl-ACP.
Der Butyrylrest unterscheidet sich vom Acetylrest durch zwei zusätzliche -CH2-Gruppen. Das Butyryl-ACP wird nunmehr in einer zweiten Runde mit Malonyl-ACP gekoppelt, und die gesamte Reaktionskette wird erneut durchlaufen. Als Folge entsteht ein Fettsäurerest, der zwei -CH2-Gruppen mehr als der Butyrylrest enthält. Erneut kann Malonyl-ACP gebunden werden, und wieder kommt es nach Durchlaufen der Reaktionskette zu einer Kettenverlängerung um eine C2-Einheit. Das kann noch einige Male so gehen, wobei jedesmal zwei -CH2-Gruppen aufgenommen werden. Das erklärt, warum die Zahl der Kohlenstoffatome in Fettsäuren immer geradzahlig ist. Beliebig lang kann die Kette auf diese Weise allerdings nicht werden, bei C16 ist Schluß. Vorläufiges Endprodukt der Fettsäuresynthese ist demnach die Palmitinsäure. Für weitergehende Verlängerungen treten andere Mechanismen in Kraft.
Die hier skizzierten Umsetzungen spielen sich alle an einem Multienzymkomplex, der Fettsäuresynthetase (siehe oben), ab. Es handelt sich dabei um ein Enzym mit einer Anzahl aktiver Zentren. Bei der Hefe besteht es aus nur zwei Polypeptidketten, die ihrerseits von nur einem Gen codiert werden. Die Trennung in die beiden Ketten erfolgt während ihres Syntheseprozesses. Das ACP ist im Zentrum des Komplexes verankert und nimmt die Funktion eines Rades wahr.
Dabei wird das an seinem äußeren Ende hängende Substrat (bzw. Produkt), zunächst also der Malonylrest, sukzessive an den einzelnen aktiven Zentren vorbeigedreht, so daß nach einem Umlauf die Kette, um eine C2-Einheit verlängert, räumlich an der gleichen Stelle angelangt ist und das Ganze von neuem beginnen kann. Der große Vorteil eines solchen Multienzymkomplexes liegt in der Vermeidung von Diffusionsverlusten und der zügigen Weiterleitung eines jeden Zwischenprodukts zum folgenden (benachbarten) aktiven Zentrum. Energiesparend ist das Verfahren auch.
Viele Fettsäuren enthalten Doppelbindungen (= ungesättigte Fettsäuren). Sie entstehen aus den gesättigten, und der Wasserstoff wird von NAD+ übernommen. Die Bildung der Doppelbindung erfolgt streng stereospezifisch. Bei den meisten Umsetzungen kommt eine cis-Bindung zustande, doch gibt es auch Enzyme, die trans-Bindungen in das Molekül einführen können.
Neben dem beschriebenen klassischen Weg der Fettsäuresynthese sind bei verschiedenen Organismengruppen Wege nachgewiesen worden, die andere Zwischenprodukte oder kurzkettige ungesättigte Fettsäuren verarbeiten. So kann z.B. die Dodecatriensäure (12 C-Atome lang, drei Doppelbindungen) - um drei Acetyleinheiten verlängert - in die Linolensäure (18:3) überführt werden. Dieser Weg wurde in Mitochondrien und im Cytosol nachgewiesen, findet vermutlich aber auch in Chloroplasten statt. In den Glykolipiden verschiedener Pflanzenarten wurden ungleiche Mengen an 18:3- und 16:3-Fettsäuren festgestellt. Man unterscheidet daher die 18:3-Pflanzen, deren Fettsäurereste mit Dreifachbindung stets 18 C-Atome lang sind, von den 16:3-Pflanzen, die sowohl C16- als auch C18-Fettsäuren enthalten. Das Verhältnis 16:3/18:3 unterliegt einer breiten artspezifischen Schwankung.
Anteil von C16- und C18-Fettsäuren in Monogalactosyldiglyceriden bei 18:3-Pflanzen (oben) und 16:3-Pflanzen (unten). Jedes Lipidmolekül enthält zwei Fettsäurereste. Mindestens einer davon ist eine C16-Fettsäure (Nach J. P. WILLIAMS et al., 1983)
Lipidfluß zwischen Membranen verschiedener Kompartimente. In grünen Pflanzen werden Fettsäuren (FS) stets in den Plastiden synthetisiert. Phospholipide (PL) werden vornehmlich im endoplasmatischen Retikulum (ER) gebildet, eine gewisse Menge entsteht auch in den Mitochondrien (Nach T. S. MOORE und G. D. TROYER, 1983)
Fette entstehen aus den Fettsäuren durch Übertragung des Fettsäurerests auf Glycerin unter Abspaltung von ACP und Ausbildung einer neuen Esterbindung (die Bindung an ACP war ebenfalls eine). Die einzelnen Typen konnten aufgrund unterschiedlicher Synthesewege drei Klassen zugeordnet werden:
Die Klasse A wird durch die Glykolipide repräsentiert. Sie stellen den Hauptteil der Chloroplastenlipide. Lipide der Klasse B sind mit Nukleotidphosphat-gekoppeltem Alkohol verknüpft. Sie machen den Hauptanteil der Lipide in Mitochondrien und cytoplasmatischen Membranen aus. Die Synthese erfolgt im Cytosol. Die Klasse C repräsentiert Nukleotiddiphosphatdiglyceride, die mit einem Alkohol verbunden sind. Hauptbildungsort dieser Gruppe ist eine Mikrosomenfraktion (aus dem Cytosol). Einige der Reaktionsschritte laufen vermutlich auch in Mitochondrien ab.
Dieser kurze Abriß weist auf die Bedeutung der Kompartimente als voneinander getrennte Reaktionsräume hin.
Abbauwege: Die Abbauwege von Lipiden sind mindestens ebenso wichtig wie die Aufbauwege, denn viele Lipide sind Speicherstoffe. Sie dienen der Zelle als Energiespeicher und müssen bei Bedarf aktiviert werden. Der Abbau ist nicht die Umkehr der Synthese, obwohl beim Abbau in der Regel C2-Einheiten (Acetylreste, die auf CoA übertragen werden) mit anfallen. Man spricht hier von beta-Oxydation. Die beteiligten Enzyme gehören in die Gruppe der Lipasen. Anfallende Protonen und Elektronen werden vom FAD und NAD+ übernommen. Citrat wirkt als Aktivator der Synthese und als Inhibitor des Abbaus. Es entsteht nur dann im Überschuß, wenn der Citratzyklus zu schnell anläuft (Acetyl-CoA-Überschuß). Ein zu zügiger Ablauf bedeutet aber auch, daß zu viel energiereiche Substanzen verbraucht und dabei in Energie überführt werden, die womöglich nicht sinnvoll verwertet werden kann. ökonomischer ist es daher, den Reservestoffabbau zu stoppen und statt dessen Acetyl-CoA in Richtung Fettsäuresynthese zu schleusen.
Neben der beta-Oxydation kommt z.B. in Samen und in Blättern auch eine alpha-Oxydation vor. Es entstehen dabei zunächst alpha-Hydroxyfettsäuren. In einem weiteren Schritt wird Kohlendioxyd abgetrennt. Es verbleibt eine um eine Cl-Einheit verkürzte Fettsäure. Zusammenfassend (Synthese gegen Abbau):
| Die Synthese erfolgt im Cytosol, der Abbau in der mitochondrialen Matrix. | |
| Die Intermediärprodukte der Synthese sind kovalent an ACP gebunden, während die Abbauprodukte (Acetylreste) an CoA gekoppelt werden. | |
| Die enzymatischen Aktivitäten der Synthese sind zu einem Multienzymkomplex, der Fettsäuresynthetase, vereint. Die für den Abbau benötigten Enzyme hängen strukturell nicht miteinander zusammen. | |
| Die Fettsäurekette wächst bei jedem Umlauf um eine C2-Einheit. Mit der Verlängerung ist eine Kohlendioxyd Freisetzung verbunden. | |
| Protonen- und Elektronendonator der Fettsäuresynthese ist das NADPH + H+ | |
| Die Fettsäuresynthese endet mit der Bildung von Palmitinsäure (C16). Eine weitere Verlängerung der Kette und das Einbringen von Doppelbindungen erfolgt unter Beteiligung anderer Enzyme. |
Andere Lipide
Die Synthese einer umfangreichen Gruppe pflanzlicher Lipide sowie
Verbindungen mit Lipidcharakter geht vom Isopren aus. Zahlreiche
der dabei gebildeten Produkte können nicht mehr dem Primärstoffwechsel
zugeschrieben werden. Weiteres dazu:
|
|